autor : Dr hab. n. med. prof. nadzw. Hanna Wolska
Mimo, że tytuł artykułu sugeruje, iż zostaną przedstawione całkowicie nowe dane dotyczące leczenia izotretynoiną, to jednak należy Czytelnika uprzedzić, że podstawowe fakty dotyczące terapii tym lekiem nie uległy zmianie. I to jest najbardziej fascynujące. Otóż, izotretynoina w terapii trądziku jest stosowana od 40 lat! W tym czasie, np. w łuszczycy wprowadzono szereg zupełnie nowych, prawie rewolucyjnych leków – takich jak cyklosporyna, a potem leki biologiczne, podczas gdy od momentu wprowadzenia izotretynoiny do leczenia trądziku nie wynaleziono żadnego, nowego, lepszego leku w tym wskazaniu! Parę miesięcy temu ukazało się opracowanie dotyczące zasad stosowania poszczególnych leków i terapii w trądziku z powołaniem się na dowody naukowe świadczące o ich skuteczności.(1) Pomimo że jest to opracowanie przygotowane przez autorów amerykańskich, to jednak w Europie istnieje z reguły zgodność poglądów odnośnie terapii trądziku ze standardami amerykańskimi. Z tego względu wydaje się, że warto przybliżyć polskiemu Czytelnikowi najnowsze dane na ten temat. Jednakże, jak wspomniano, zasadnicze fakty dotyczące izotretynoiny nie zmieniły się, przypominając je pokrótce, przy omawianiu poszczególnych aspektów leczenia izotretynoiną znajdą się odniesienia do powyższego opracowania.
Co to jest izotretynoina?
Izotretynoina – kwas 13-cis witaminy A jest naturalnym, obok kwasu all-trans, retinoidem występującym w organizmie. Powstaje ona w wątrobie na drodze metabolizmu wchłoniętej z przewodu pokarmowego witaminy A lub karotenoidu będącego prowitaminą A.
Podobnie jak i inne retinoidy, działanie jej zachodzi poprzez wiązanie się z receptorami jądrowymi, które należą do nadrodziny czynników transkrypcyjnych jądrowego DNA i są pobudzane w podobnym mechanizmie przez hormony steroidowe, hormony tarczycy, witaminę D. Retinoidy wywierają swój wpływ na tkanki docelowe wiążąc się z nośnikiem białkowym – CRABP I i II (ang. cellular retinoid binding protein), który umożliwia ich połączenie ze swoistymi receptorami jądrowymi (RAR, RXR). Ponieważ izotretynoina nie wiąże się z CRBP I czy II zakłada się, że sama ona nie jest aktywna biologicznie, a działa jako pro-lek, podczas gdy biologiczne efekty są zależne od jej metabolitów, głównie kwasu all-trans.(2,3) Wykazano, że przemiana izotretynoiny w tretynoinę zachodzi szczególnie szybko w sebocytach, a nie w keratynocytach.(4) Tłumaczyć to może unikalne działanie izotretynoiny na gruczoły łojowe.
Izotretynoina jest łatwiej wchłaniana w obecności tłuszczów, więc lepiej przyjmować ją w czasie posiłku.
Doustne podawanie izotretynoiny zmniejsza wymiary gruczołów łojowych i ilość wydzielanego łoju, która ulega obniżeniu 10-krotnie, a ponadto normalizuje rogowacenie ujść mieszków włosowych. Oba procesy zapobiegają tworzeniu nowych zaskórników, czego wynikiem jest zahamowanie wzrostu populacji Propionibacterium acnes i działanie przeciwzapalne.(5)
Podstawowe wskazania do zastosowania izotretynoiny
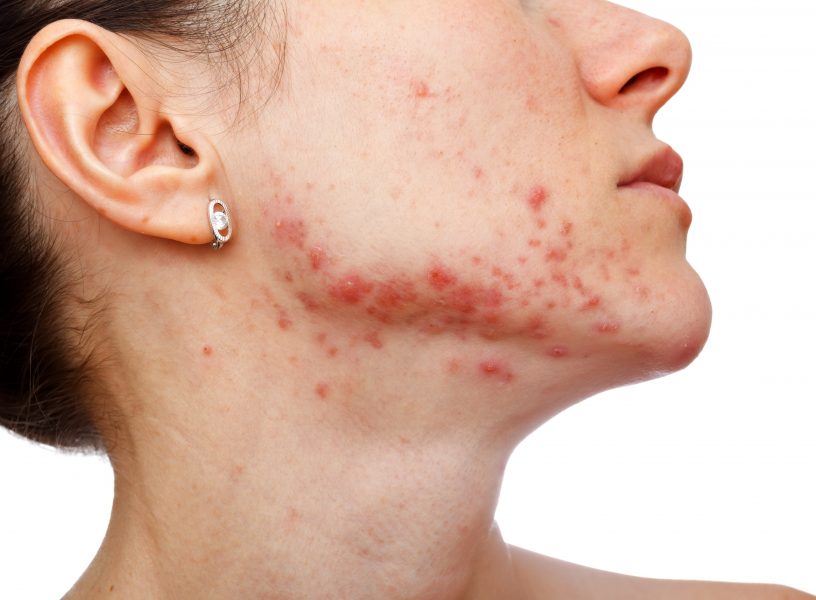
Podstawowe wskazanie do stosowania izotretynoiny stanowi trądzik.
Wynika to z mechanizmu działania leku, gdyż izotretynoina wpływa na wszystkie zjawiska odgrywające rolę w patogenezie zmian trądzikowych:
– przerost gruczołów łojowych i zwiększoną produkcję łoju;
– tworzenie się zaskórników (lek powoduje normalizację procesów rogowacenia w obrębie mieszków łojowo-włosowych; pośrednio wpływa na zmniejszenie liczby P. acnes, na skutek stwarzania gorszych warunków dla ich rozwoju);
– odczyn zapalny.
Od końca lat 70-tych do połowy 80-tych izotretynoinę stosowano wyłącznie w najcięższych postaciach trądziku – acne conglobata, cystica.(2) Światowe doświadczenie z lekiem pozwoliło na rozszerzenie wskazań do jego zastosowania.(2,6) Obecnie wskazania do leczenia izotretynoiną w trądziku obejmują:
- acne phlegmonosa (cystica, nodulo-cystica, conglobata);
- średnio-bardzo nasilony trądzik niepoddający się terapii antybiotykami lub z bardzo szybkimi nawrotami;
– średnio-bardzo nasilony trądzik z bardzo dużym łojotokiem, tendencją do bliznowacenia;
– średnio nasilony trądzik stanowiący dla pacjenta duże obciążenie psychiczne.(1,2)
Dawkowanie
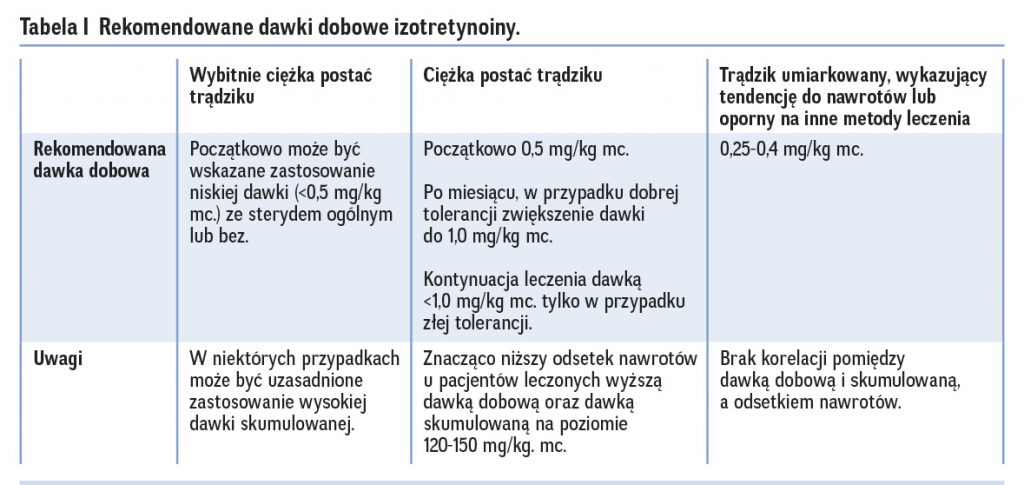
Nadal utrzymują się w mocy zalecenia odnośnie kumulacyjnej dawki izotretynoiny. Istotne jest, ażeby łączna dawka preparatu podczas kuracji nie była niższa niż 120 mg/kg/dz., a w przypadku bardzo nasilonych zmian, zwłaszcza na plecach nawet 150 mg/kg/dz.. Wynika to z obserwacji, iż dopiero podanie takich dawek w istotny sposób redukuje ryzyko nawrotu trądziku.(1,2) Nie wydaje się natomiast, żeby przekraczanie tej dawki wpływało korzystnie na częstość nawrotów. Dotychczas dzienne dawki preparatu wahały się od 0.1 – 0.5 –1.0 mg/kg/dz. i uzależnione były głównie od klinicznych objawów niepożądanych.(2) Obserwacje i badania ostatnich lat wykazały jednak, że stosowanie maksymalnych dawek ~1 mg/kg wpływa w sposób istotny na częstość i nasilenie nawrotów.(7) W związku z powyższym zaleca się obecnie rozpoczynanie terapii od dawki 0.5 mg/kg/dz. stosowanej przez miesiąc, a następnie zwiększanie jej, oczywiście z uwzględnieniem tolerancji pacjenta, do dawki maksymalnej ~1 mg/kg/dz. do końca leczenia.(1)
U pacjentów z trądzikiem o szczególnie ciężkim przebiegu, ze względu na ryzyko rozwoju acne fulminans w początkowym okresie leczenia może być wskazane zastosowanie niskiej dawki dobowej izotretynoiny (<0.5 mg/kg mc.) ze sterydem ogólnym lub bez.(1) Stwierdzono, że wysoka dawka kumulacyjna u tych pacjentów (>220 mg/kg mc.) może skutkować niższym wskaźnikiem nawrotów (wniosek wymaga potwierdzenia w badaniach na większej populacji).(19,20)
Istotne novum dotyczy średnio nasilonego trądziku, opornego na leczenie antybiotykami lub bardzo szybko nawracającego po turze antybiotyków. Wykazano, że w tych przypadkach skuteczne jest podawanie izotretynoiny w dawkach 0.25-0.4 mg/kg/dz..(1,8,9) Co istotne, w średnio nasilonym trądziku powyższa metoda leczenia, nawet bez osiągnięcia kumulacyjnej, standardowej dawki nie skutkuje zwiększeniem częstości nawrotów.(1)
Bezwzględnie natomiast nie zaleca się terapii przerywanej, gdyż w sposób istotny wpływa ona na zwiększenie ich częstości i nasilenia.(9,10)
Objawy niepożądane
Teratogenność
Najniebezpieczniejszym działaniem niepożądanym izotretynoiny jest jej teratogenność. Izotretynoina, tak jak i inne pochodne witaminy A podana w okresie ciąży może prowadzić do poronienia, porodu przedwczesnego lub do bardzo ciężkiego uszkodzenia płodu objawiającego się uszkodzeniem czaszki, narządu słuchu oraz wad w obrębie układu naczyniowo-sercowego. Ponieważ objawy te występują tylko podczas obecności retinoidów w organizmie, a izotretynoina jest wydalana w przeciągu 2-4 tyg. po zaprzestaniu jej podawania, zalecany okres unikania ciąży po zakończeniu kuracji wynosi ~4 tyg.. Za standardowe postępowanie prewencyjne przyjmuje się obecnie stosowanie przez kobiety i przez mężczyzn dwóch metod antykoncepcji lub wręcz przestrzeganie zasad abstynencji.
Z tym, że należy zaznaczyć, że u mężczyzn izotretynoina nie wpływa uszkadzająco na spermatogenezę.(1,2)
Kliniczne działania niepożądane
Najczęstszymi objawami niepożądanymi, które w większości przypadków wpływają na ustalenie dawki tolerowanej przez pacjenta są objawy skórno-śluzówkowe związane z wysychaniem. Najczęściej dotyczy to czerwieni wargowej (złuszczanie, pęknięcia, zajady), o wiele rzadziej wysychania śluzówki nosa, z którym mogą łączyć się niewielkie krwawienia. Bardzo rzadko, ale mogą również wystąpić krwawienia ze śluzówki odbytu. Najgroźniejsza jest możliwość wystąpienia suchości w obrębie spojówek, która jednakże, na szczęście, zdarza się najrzadziej. W przypadkach takich obawiamy się nadkażenia bakteryjnego, zwłaszcza Staphylococcus aureus, co może być groźne dla narządu wzroku. Suchość połączoną z rumieniem i złuszczaniem obserwuje się najczęściej w obrębie skóry twarzy. W innych okolicach, przeważnie na kończynach górnych może dojść do pojawienia się zmian przypominających różnego typu ogniska wypryskowe, najczęściej typu powierzchownego eczema nummulare.(1,2)
W czasie leczenia izotretynoiną najbardziej dokuczliwy dla pacjentów objaw związany z leczeniem retinoidami – wypadanie włosów pod postacią rozlanego łysienia – obserwuje się rzadko.
Poza wymienionymi objawami podczas terapii retinoidami mogą pojawić się bóle stawowe i mięśniowe, objawy zmęczenia, rzadko świąd.
Na szczególną uwagę zasługuje kilka potencjalnych działań niepożądanych. Ze względu na pojedyncze doniesienia o występowaniu tendencji samobójczych i dokonanych samobójstwach w grupie osób leczonych izotretynoiną przeprowadzono w ostatnich latach szereg analiz, w których nie stwierdzono związku przyczynowego pomiędzy przyjmowaniem izotretynoiny a skłonnością do depresji.(1,11) Wręcz przeciwnie, w niektórych badaniach wykazano wręcz korzystny wpływ izotretynoiny na stan psychiczny.(1,11) Nie mniej, ze względu na częste występowanie depresji zwłaszcza u młodych osób z najcięższym trądzikiem, którzy są kandydatami do terapii izotretynoiną, podkreśla się konieczność dokładnej obserwacji tych chorych.(1,2)
Izotretynoina może dawać zmiany w układzie kostnym, ale należy zaznaczyć, że są one głównie opisywane po przewlekłym, wieloletnim podawaniu, np. u chorych z chorobami z kręgu zaburzeń rogowacenia. Poza dwoma doniesieniami o przedwczesnym zarośnięciu nasad kostnych u osób leczonych izotretynoiną z powodu trądziku nie potwierdzono tego zjawiska w innych obserwacjach. W związku z powyższym autorzy ostatniego konsensusu uważają, że podczas leczenia trądziku nie zachodzi konieczność monitorowania układu kostnego.(1) Kolejnym teoretycznym powikłaniem leczenia izotretynoiną jest rozwój zapalnej choroby jelit (ang. Inflammatory Bowel Disease, IBD), co opisywano w pojedynczych badaniach.(12,13) Nie mniej późniejsze doniesienia nie wykazały jakiegokolwiek związku przyczynowego pomiędzy przyjmowaniem izotretynoiny a IBD.(14,15) Trochę kontrowersyjne jest w doniesieniu amerykańskim przedstawienie jeszcze innego problemu, a mianowicie opóźnionego gojenia ran i powstawania blizn u osób aktualnie lub niedawno leczonych izotretynoiną. Autorzy dają przykłady doniesień, z których wynika, że nie występuje niebezpieczeństwo nietypowego gojenia lub bliznowacenia u osób leczonych izotretynoiną poddawanych takim zabiegom jak pilingi chemiczne, ręczna dermabrazja, różnego typu zabiegi laserowe.(16,17,18) Prace te oparte są jednak na małym materiale i sami autorzy ostatnich zaleceń podkreślają zasadność wstrzymywania się generalnie od zabiegów kosmetycznych przez 6-12 miesięcy po leczeniu izotretynoiną, z tym, że dopuszczają możliwość wykonywania takich zabiegów w pojedynczych przypadkach.
Odchylenia w wynikach badań laboratoryjnych
Izotretynoina może powodować zwyżki aktywności transaminaz u <10% leczonych i, częściej, zmiany w poziomach lipidów (u~30%) polegające na zwyżce stężenia cholesterolu i trójglicerydów, a także na niekorzystnym wpływie na poszczególne frakcje cholesterolu – obniżeniu poziomu HDL i zwiększeniu poziomu LDL. Z tego względu cały czas zalecane jest sprawdzenie przed leczeniem tych wskaźników oraz ich monitorowanie w trakcie terapii. Jednakże odchylenia te stwierdza się głównie u pacjentów, u których w badaniach wyjściowych występowały wartości podwyższone. Ponadto szczególnie wskazana jest ich kontrola u pacjentów z czynnikami ryzyka takimi jak: nadwaga, hiperlipidemia w wywiadzie lub w rodzinie, cukrzyca. Zwyżki transaminaz i lipidów ulegają normalizacji po ~2 mies. od zaprzestania terapii.(1,2) Nie wydaje się natomiast konieczne regularne monitorowanie morfologii krwi.(1)
Postępowanie w trakcie terapii izotretynoiną
Najważniejsze jest rygorystyczne zapobieganie ciąży w trakcie terapii i do czterech tygodni od jej zaprzestania. Istotne jest uświadomienie pacjentce zagrożeń związanych z terapią izotretynoiną i uzyskanie podpisu pod oświadczeniem potwierdzającym zrozumienie tych zagrożeń. Ponieważ już po kilku dniach od rozpoczęcia terapii u większości pacjentów występuje zmniejszenie łojotoku (w tym przetłuszczania włosów) i wyraźne wysuszenie skóry nie zaleca się jednoczesnego stosowania leczenia miejscowego. Aplikacja miejscowych preparatów z retinoidami lub nadtlenkiem benzoilu może wręcz nasilić występujące podczas leczenia izotretynoiną działania niepożądane. Jednocześnie właśnie ze względu na znaczną suchość skóry i śluzówek występującą podczas leczenia zaleca się od początku terapii stosowanie preparatów natłuszczających wargi, a w razie wystąpienia suchości skóry stosowanie łagodnych, obojętnych preparatów nawilżających. Osoby noszące szkła kontaktowe powinny stosować szczególnie często preparaty nawilżające spojówki, ale najlepiej jest zaprzestać ich stosowania podczas terapii.
W przypadku planowanej ekspozycji na słońce pacjenci leczeni izotretynoiną powinni stosować silne preparaty ochronne przed UV. Nie wynika to z fotouczulających własności leku tylko ze zwiększonej wrażliwości skóry podczas leczenia retinoidami.
W trakcie leczenia nie należy stosować tetracyklin, preparatów z wit. A, metotreksatu. Należy unikać spożywania alkoholu. Konieczna jest obserwacja stanu psychicznego pacjenta, a w razie wystąpienia objawów depresji odstawienie leku i konsultacja psychiatryczna.(1,2)
Podsumowując, wydaje się, że zarówno obserwacje dnia codziennego, jak i dane z badań porównawczych potwierdzają nie tylko wybitną skuteczność izotretynoiny w leczeniu najcięższych postaci trądziku, ale również bezpieczeństwo tej terapii, oczywiście pod warunkiem przestrzegania podstawowych zasad związanych z jej prowadzeniem.
Warto pamiętać ponadto, że izotretynoina znajduje zastosowanie nie tylko w różnie nasilonym trądziku zwyczajnym, ale również w szeregu innych schorzeń. Do najważniejszych należą: acne fulminans, acne inversa (hidradenitis suppurativa), rosacea, nasilony łojotok, Gram negative folliculitis i choroby przebiegające z nadmiernym rogowaceniem – wrodzone i nabyte.(2) Leczenie izotretynoiną w tych wskazaniach przebiega jednak inaczej niż w acne vulgaris. Dotyczy to zwłaszcza zaburzeń rogowacenia, w których, w przeciwieństwie do trądziku, terapia bywa długotrwała – często wieloletnia. Nie mniej większość przedstawionych w obecnym opracowaniu zasad leczenia izotretynoiną również ma tam miejsce.
Piśmiennictwo
1. Work Group: Zaenglein A.L., Pathy A.L., Schlosser B.J. i wsp.: Guidelines of care for the management of acne vulgaris. J Am Acad Dermatol 2016, 74, 945-973.
2. Wolska H., Gliński W.: Zastosowanie doustnej izotretynoiny w dermatologii. Przegl Dermatol 2005, 92, 407-412.
3. Zouboulis C.C., Orfanos C.E.: Retinoids. [w:] Drug therapy in dermatology. Millikan L.E. (red.) Marcel Dekker, Inc., New York, 2000, 171-233.
4. Tsukada M., Schroder M., Roos T. I wsp.: 13-cis retinoic acid exerts its specific activity on human sebocytes through selective intracellular isomerization to all-trans retinoic acid and binding to retinoic acid receptors. J Invest Dermatol 2000, 115, 322-327.
5. Pawin H., Beylot C., Chivot M. i wsp.: Physiopathology of acne vulgaris: recent data, new understanding of the treatments. Eur J Dermatol 2004, 14, 4-12.
6. Gollnick H., Cunliffe W., Bernson D. i wsp.: Management of acne. A report from a global alliance to improve outcomes in acne. J Am Acad Dermatol 2003,49:31-38.
7. Goldsmith L.A., Bolognia J.L., Callen J.P. i wsp.: American Academy of Dermatology Consensus Conference on the safe and optimal use of isotretinoin: summary and recommendations. J Am Acad Dermatol 2004, 50, 900-906.
8. Amichai B., Shemer A., Grunwald M.H.: Low-dose isotretinoin in the treatment of acne vulgaris. J Am Acad Dermatol 2006, 54, 644-646.
9. Agarwal U.S., Besarwal R.K., Bhola K.: Oral isotretinoin in different dose regimens for acne vulgaris: a randomized comparative trial. Indian J Dermatol Venereol Leprol 2011, 77, 688-694.
10. Akman A., Durusoy C., Senturk M. i wsp.: Treatment of acne with intermittent and conventional isotretinoin: a randomized, controlled multicenter study. Arch Dermatol Res 2007, 299, 467-473.
11. Marqueling A.L., Zane L.T.: Depression and suicidal behavior in acne patients treated with isotretinoin: a systemic review. Semin Cutan Med Surg 2005, 24, 92-102.
12. Reddy D., Siegel C.A., Sands B.E., Kane S.: Possible association between isotretinoin and inflammatory bowel disease. Am J Gastroenterol 2006, 101, 1569-1573.
13. Dubeau M.F., Iacucci M., Beck P.L. i wsp: Drug-induced inflammatory bowel disease and IBD-like conditions. Inflamm Bowel Dis 2013, 19, 445-456.
14. Etminan M., Bird S.T., Delaney J.A. i wsp: Isotretinoin and risk for inflammatory bowel disease: a nested case-control study and meta-analysis of published and unpublished data. JAMA Dermatol 2013, 149, 216-220.
15. Rahstak S., Khaleghi S., Pittelkow M.R. i wsp: Isotretinoin exposure and risk of inflammatory bowel disease. JAMA Dermatol 2014, 150, 12, 1322-1326.
16. Picosse F.R., Yarak S., Cabral N.C., Bagatin E.: Early chemabrasion for acne scars after treatment with oral isotretinoin. Dermatol Surg 2012, 38, 1521-1526.
17. Chandrashekar B.S., Varsha D.V., Vasanth V. i wsp.: Safety of performing invasive acne scar treatment and laser hair removal in patients on oral isotretinoin: a retrospective study of 110 patients. Int J Dermatol 2014, 53, 1281-1285.
18. Kim H.W., Chang S.E., Kim J.E. i wsp.: The safe delivery of fractional ablative carbon dioxide laser treatment for acne scars in Asian patients receiving oral isotretinoin. Dermatol Surg 2014, 40, 1361- 1366.
19. Cyrulnik A: High-Dose Isotretinoin (Accutane) Therapy: Positive Results in Nodulocystic Acne. American Academy of Dermatology, Meeting Highlights. P&T May 2011, Vol. 36 No. 5: 294.3.
20. Blasiak RC i wsp.: High-dose isotretinoin treatment and the rate of retrial, relapse, and adverse effects in patients with acne vulgaris. JAMA Dermatol. 2013;149:1392-1398.
Artykuł ukazał się na łamach Dermatologii i Kosmetologii Praktycznej Vol. 13. Nr 1 (47)